|
Началась новая эра редактирования митохондриального генома
|
| Исследователи из Центра инженерии генома Института фундаментальных наук разработали новую платформу для редактирования генов, называемую эффекторно-связанными деаминазами, подобными активатору транскрипции, или TALED. TALED — это редакторы оснований, способные выполнять преобразование оснований A в G в митохондриях. Это открытие стало кульминацией многолетнего пути к излечению генетических заболеваний человека, и TALED можно считать последней недостающей частью головоломки в технологии редактирования генов. |
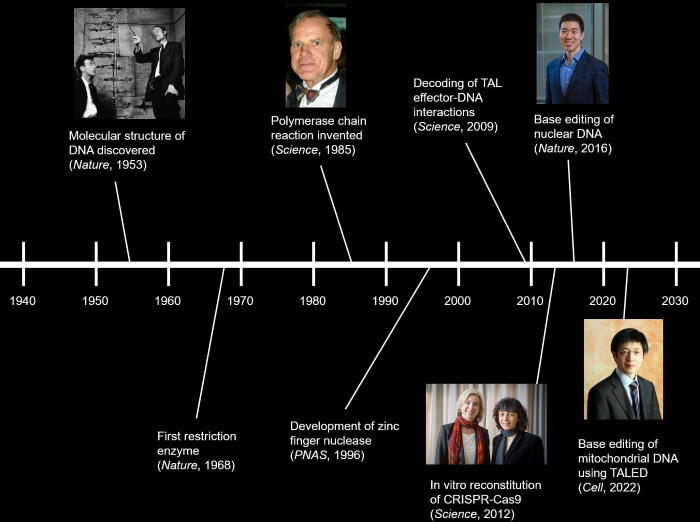
| Начиная с идентификации первого фермента рестрикции в 1968 г., изобретения полимеразной цепной реакции (ПЦР) в 1985 г. и демонстрации редактирования генома с помощью CRISPR в 2013 г., каждое новое прорывное открытие в биотехнологии еще больше улучшало нашу способность манипулировать ДНК, схема жизни. В частности, недавняя разработка системы CRISPR-Cas, или «генетических ножниц», позволила проводить всестороннее редактирование генома живых клеток. Это открыло новые возможности для лечения ранее неизлечимых генетических заболеваний путем удаления мутаций из нашего генома. |
|
| В то время как редактирование генов было в значительной степени успешным в ядерном геноме клеток, однако ученым не удалось отредактировать митохондрии, которые также имеют свой собственный геном. Митохондрии, так называемые «электростанции клеток», представляют собой крошечные органеллы в клетках, которые служат фабриками по производству энергии. Поскольку это важная органелла энергетического метаболизма, мутация гена вызывает серьезные генетические заболевания, связанные с энергетическим обменом. |
| Директор Центра инженерии генома Ким Джин-Су объяснил: «Существуют очень неприятные наследственные заболевания, возникающие из-за дефектов митохондриальной ДНК. Например, наследственная оптическая нейропатия Лебера (LHON), вызывающая внезапную слепоту на оба глаза, простой точечной мутацией в митохондриальной ДНК». Другое заболевание, связанное с митохондриальными генами, включает митохондриальную энцефаломиопатию с лактоацидозом и инсультоподобными эпизодами (MELAS), которая медленно разрушает мозг пациента. Некоторые исследования даже предполагают, что аномалии в митохондриальной ДНК также могут быть причиной дегенеративных заболеваний, таких как болезнь Альцгеймера и мышечная дистрофия. |
| Митохондриальный геном наследуется по материнской линии. Известно 90 точечных мутаций митохондриальной ДНК, вызывающих болезни, которые в общей сложности затрагивают не менее 1 из 5000 человек. Многие существующие инструменты редактирования генома нельзя было использовать из-за ограничений метода доставки в митохондрии. Например, платформа CRISPR-Cas неприменима для редактирования этих мутаций в митохондриях, поскольку направляющая РНК не может проникнуть в саму органеллу. |
| «Еще одна проблема заключается в том, что существует нехватка животных моделей этих митохондриальных заболеваний. Это связано с тем, что в настоящее время невозможно сконструировать митохондриальные мутации, необходимые для создания животных моделей», — добавил директор Ким. «Отсутствие моделей на животных очень затрудняет разработку и тестирование терапевтических средств для этих заболеваний». Таким образом, надежная технология редактирования митохондриальной ДНК является одним из последних рубежей геномной инженерии, которую необходимо изучить, чтобы победить все известные генетические заболевания, и самые элитные ученые мира годами пытались воплотить ее в жизнь. |
| В 2020 году исследователи под руководством Дэвида Р. Лю из Института Броуда Гарварда и Массачусетского технологического института создали новый базовый редактор, названный редакторами оснований цитозина, производными от DddA (DdCBE), который может выполнять преобразование C-to-T из ДНК в митохондриях. Это стало возможным благодаря созданию новой технологии редактирования генов, называемой редактированием оснований, которая преобразует одно нуклеотидное основание в другое без нарушения ДНК. Однако и эта техника имела свои ограничения. Он не только ограничен преобразованием C в T, но и в основном ограничен мотивом TC, что делает его эффективным преобразователем TC-TT. Это означает, что он может исправить только 9 из 90 (= 10%) подтвержденных патогенных митохондриальных точечных мутаций. Долгое время считалось, что преобразование митохондриальной ДНК из A в G невозможно. |
| Первый автор Чо Сон-Ик сказал: «Мы начали думать о способах преодоления этих ограничений. В результате мы смогли создать новую платформу редактирования генов под названием TALED, которая может достичь преобразования A в G. Наша новая база редактор значительно расширил возможности редактирования митохондриального генома. Это может внести большой вклад не только в создание модели болезни, но и в разработку лечения». Следует отметить, что возможность выполнять преобразования A-G в одной только мтДНК человека может исправить 39 (= 43%) из 90 известных патогенных мутаций. |
| Исследователи создали TALED, объединив три разных компонента. Первый компонент представляет собой эффектор, подобный активатору транскрипции (TALE), который способен нацеливаться на последовательность ДНК. Вторым компонентом является TadA8e, адениндезаминаза для облегчения превращения A в G. Третий компонент, DddAtox, представляет собой цитозиндезаминазу, которая делает ДНК более доступной для TadA8e. |
| Одним из интересных аспектов TALED является способность TadA8e выполнять редактирование от A до G в митохондриях, которые обладают двухцепочечной ДНК (dsDNA). Это загадочное явление, поскольку TadA8e — это белок, который, как известно, специфичен только для одноцепочечной ДНК. Директор Ким сказал: «Раньше никому не приходило в голову использовать TadA8e для редактирования оснований в митохондриях, поскольку предполагается, что он специфичен только для одноцепочечной ДНК. Именно этот нестандартный подход действительно помог нам изобрести СКАЗАЛ." |
| Исследователи предположили, что DddAtox позволяет сделать двухцепочечную ДНК доступной за счет кратковременного раскручивания двойной цепи. Это мимолетное, но временное временное окно позволяет TadA8e, сверхбыстродействующему ферменту, быстро вносить необходимые изменения. В дополнение к настройке компонентов TALED исследователи также разработали технологию, которая позволяет одновременно редактировать базу A-to-G и C-T, а также только базовое редактирование A-to-G. |
| Группа продемонстрировала эту новую технологию, создав единственный клеточный клон, содержащий желаемые модификации мтДНК. Кроме того, было обнаружено, что TALED не являются цитотоксическими и не вызывают нестабильности мтДНК. Кроме того, не было нежелательного нецелевого редактирования в ядерной ДНК и очень мало нецелевых эффектов в мтДНК. Теперь исследователи стремятся к дальнейшему совершенствованию TALED за счет повышения эффективности и специфичности редактирования, что в конечном итоге проложит путь к исправлению вызывающих болезни мутаций мтДНК у эмбрионов, плодов, новорожденных или взрослых пациентов. Группа также занимается разработкой TALED, подходящих для редактирования оснований от A до G в ДНК хлоропластов, которая кодирует важные гены фотосинтеза у растений. |
| Уильям И. Су, научный коммуникатор Института фундаментальных наук, провозгласил: «Я считаю, что значение этого открытия сравнимо с изобретением синего светодиода, за которое в 2014 году была присуждена Нобелевская премия. Последняя часть головоломки, которая позволила нам получить высокоэффективный источник белого светодиодного света, ожидается, что TALED откроет новую эру геномной инженерии». Исследование опубликовано в Cell. |
| Источник |